Parte I: Desvendando a malha de FIBRINA
- Juliana magro ribeiro
- 26 de jul. de 2016
- 3 min de leitura
O protocolo de obtenção do L-PRF foi criado pelo pesquisador Joseph Choukroun em 2001 em um trabalho intitulado: Une opportunité en paro-implantologie: Le PRF. Em 2006, um conjunto de cinco importantes artigos foram publicados pelos cientistas Choukroun, Dohan e seus colaboradores. Estes cinco trabalhos evidenciaram as características da estrutura e da biologia celular e molecular que tornam o PRF uma técnica muito interessante para a prática clínica, além de fazerem uma demonstração do uso do L-PRF em um levantamento de seio. Durante as próximas semanas trarei um resumo de cada um desses cinco trabalhos. Esses resumos funcionarão como aperitivo para a leitura do artigo na íntegra, a qual é obrigatória para o profissional que pretende beneficiar seus pacientes com o L-PRF.
O primeiro artigo é intitulado: Platelet-rich fibrin (PRF): A second-generation platelet concentrate. Part I: Technological concepts and evolution.
O protocolo desenvolvido por Chouckroun tem a matriz de fibrina como componente primordial da sua pesquisa. Mas o que seria a fibrina? A fibrina (proteína insolúvel) é o produto final da ação da trombina sobre o fibrinogênio (precursor proteico e solúvel da fibrina) durante a cascata de coagulação, como mostrado na figura.
Não é recente o uso da fibrina como cola biológica em várias cirurgias da área da saúde. Os adesivos de fibrina são principalmente conhecidos pela sua utilização na vedação das bordas da ferida e pela facilitação da aplicação cutânea em cirurgia geral, plástica e buco-maxilo-facial. Assim, esses profissionais utilizam as propriedades mecânicas do adesivo, bem como as propriedades biológicas da fibrina, para promoverem a cicatrização. No entanto, por vários anos não havia um protocolo satisfatório quanto à segurança contra infecções por doenças transmitidas pelo sangue, satisfatório no preço para obtenção do produto, satisfatório na reprodutibilidade dos resultados científicos e que fosse prático para ser implementado da rotina dos consultórios.
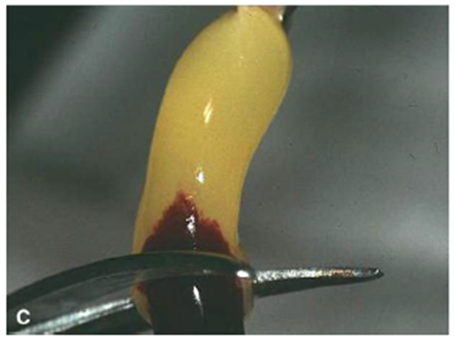
Um dos produtos utilizados para fins científicos e até mesmo na prática clínica foi o Plasma Rico em Plaquetas (PRP). Nesse protocolo, quando era necessário que o PRP formasse uma matriz, trombina bovina e cloreto de cálcio eram adicionados ao PRP, que já havia passado por uma centrifugação para retirada do plasma pobre em plaquetas e eram descartadas as hemácias. É nesta fase de adição de cloreto de cálcio e trombina bovina que as citocinas de plaquetas são normalmente liberadas. O grupo de Dohan, neste primeiro artigo, compara a malha formada pelo PRP com a malha formada pela membrana de fibrina obtida com o protocolo de L-PRF. Com um protocolo simples, o L-PRF não envolve o acréscimo de trombina humana e cloreto de cálcio. O sucesso desta técnica depende inteiramente da velocidade da coleta de sangue e de início de centrifugação. Assim, a manipulação rápida é a única maneira de obter um coágulo de PRF clinicamente utilizável. Por envolver apenas os componentes fisiológicos da coagulação, PRF polimeriza de maneira natural e lenta e isso é o que permite a conformação diferenciada da matriz de fibrina do PRF. A malha de fibrina do PRF possui uma conformação que possibilita a ancoragem de citocinas e a migração celular (Figura 2). Diferentemente do que era obtido com outros protocolos, a membrana de PRF, devido a sua arquitetura, é flexível, elástica, e muito forte. Portanto, este primeiro trabalho traz de novidade que o modo de polimerização lenta confere à membrana PRF uma arquitetura fisiológica única que é muito importante para favorecer e para apoiar o processo de cicatrização. Como e quais as demais propriedades da membrana de L-PRF que favorecem a cicatrização??? Ficou com vontade de mais? Agora é só esperar o próximo post.

Figura 2: Ilustração da estrutura da malha/membrana de fibrina. A concentração de trombina fisiológica implica em uma percentagem muito significativa de inserções equiláteras. Estas junções ligadas permitem o estabelecimento de uma rede de fibrina fina e flexível capaz de suportar citocinas ancoradas e migração celular. Além disso, esta associação de três dimensões vai dar grande elasticidade para a matriz de fibrina: É o que se observa em uma membrana PRF: flexível, elástica, e muito forte
Bibliografia: Dohan, D. M., J. Choukroun, et al. (2006). "Platelet-rich fibrin (PRF): a second-generation platelet concentrate. Part I: technological concepts and evolution." Oral Surg Oral Med Oral Pathol Oral Radiol Endod 101(3): e37-44.
Figuras retiradas do mesmo trabalho.
























Comments